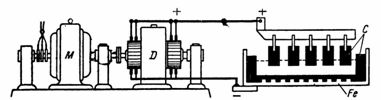
Elektroliza. Primjeri proračuna
 Elektroliza je razgradnja elektrolita (otopine soli, kiseline, baze) uz pomoć električne struje.
Elektroliza je razgradnja elektrolita (otopine soli, kiseline, baze) uz pomoć električne struje.
Elektroliza se može provoditi samo istosmjernom strujom. Tijekom elektrolize, vodik ili metal sadržan u soli oslobađa se na negativnoj elektrodi (katodi). Ako je pozitivna elektroda (anoda) metalna (obično ista kao u soli), tada se pozitivna elektroda otapa tijekom elektrolize. Ako je anoda netopljiva (npr. ugljik), tada se sadržaj metala u elektrolitu smanjuje tijekom elektrolize.
Količina tvari koja se oslobađa tijekom elektrolize na katodi proporcionalna je količini elektriciteta koji je prošao kroz elektrolit.
Količina tvari koju oslobodi jedan kulon elektriciteta naziva se elektrokemijski ekvivalent A, stoga je G = A • Q; G = A • I • t,
gdje je G količina izolirane tvari; Q je količina električne energije; I — električna struja; t je vrijeme.
Svaki metal ima svoj elektrokemijski ekvivalent A.
Primjeri proračuna
1. Koliko će se bakra osloboditi iz bakrenog sulfata (CuSO4) (slika 1) uz struju I = 10 A tijekom 30 minuta.Elektrokemijski ekvivalent bakra A = 0,329 mg / A • sek.
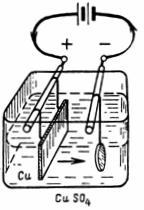
Riža. 1. Primjer sheme 1
G = A • I • t = 0,329 • 10 • 30 • 60 = 5922 mg = 5,922 g.
Predmet koji visi na katodi oslobodit će 5,9 g čistog bakra.
2. Dopuštena gustoća struje u bakrenoj elektrolitičkoj prevlaci • = 0,4 A / dm2. Površina katode koju treba pokriti bakrom je S = 2,5 dm2. Kolika je struja potrebna za elektrolizu i koliko se bakra oslobodi na katodi za 1 sat (slika 2).
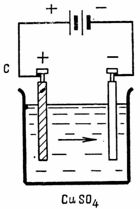
Riža. 2. Primjer sheme 2
I = •• S = 0,4-2,5 = l A; G = A • Q = A • I • t = 0,329 • 1 • 60 • 60 = 1184,4 mg.
3. Oksidirana voda (npr. slaba otopina sumporne kiseline H2SO4) tijekom elektrolize se raspada na vodik i kisik. Elektrode mogu biti ugljene, kositrene, bakrene itd., ali najbolja je platina. Koliko će se kisika osloboditi na anodi, a koliko vodika na katodi za 1/4 sata pri struji od 1,5 A. Količina elektriciteta 1 A sec oslobodi 0,058 cm3 kisika i 0,116 cm3 vodika (sl. 3).
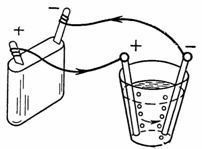
Riža. 3. Primjer sheme 3
Na katodi će se osloboditi Ga = A • I • t = 0,058 • 1,5 • 15 • 60 = 78,3 cm3 kisika.
Gc = A • I • t = 0,1162 • 1,5 • 15 • 60 = 156,8 cm3 vodika će se osloboditi na anodi.
Mješavina vodika i kisika u ovom omjeru naziva se eksplozivnim plinom, koji kada se zapali eksplodira, stvarajući vodu.
4. Kisik i vodik za laboratorijske pokuse dobivaju se pomoću elektroliza vode (oksidirana sumporna kiselina) (slika 4). Platinaste elektrode zalemljene su u staklo. Pomoću otpora postavili smo struju I = 0,5 A. (Kao izvor struje koristi se baterija od tri suha elementa od 1,9 V) Koliko će se vodika i kisika osloboditi nakon 30 minuta.
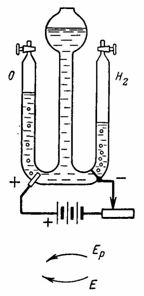
Riža. 4… Slika 4 na primjer
U desnoj posudi će se osloboditi Gc = A • I • t = 0,1162 • 0,5 • 30 • 60 = 104,58 cm3 vodika.
U lijevoj posudi će se razviti Ga = A • l • t = 0,058 • 0,5 • 30 • 60 = 52,2 cm3 kisika (plinovi istiskuju vodu u srednjoj posudi).
5. Pretvarački blok (motor-generator) daje struju za dobivanje elektrolitskog (čistog) bakra. Za 8 sati treba dobiti 20 kg meda. Koju struju treba dati generator? • Elektrokemijski ekvivalent bakra je A = 0,329 mg / A • sec.
Budući da je G = A • I • t, tada je I = G / (A • t) = 20 000 000 / (0,329 • 8 • 3600) = 20 000 000 / 9475,2 = 2110,7 A.
6. Potrebno je kromirati 200 farova od kojih je za svaki potrebno 3 g kroma. Kolika je struja potrebna da se taj rad obavi u 10 sati (elektrokemijski ekvivalent kroma A = 0,18 mg / A • s).
I = G / (A • t) = (200 • 3 • 1000) / (0,18 • 10 • 3600) = 92,6 A.
7. Aluminij se dobiva elektrolizom otopine kaolinske gline i kriolita u kupkama pri radnom naponu kupke od 7 V i jakosti struje od 5000 A. Anode su od ugljena, a kupka od čelika s ugljenom. blokovi (slika 5).
Riža. 5 Na primjer, slika 5
Kupke za proizvodnju aluminija spojene su u seriju za povećanje radnog napona (na primjer, 40 kupki). Za proizvodnju 1 kg aluminija potrebno je približno 0,7 kg ugljičnih anoda i 25-30 kWh električne energije. Na temelju zadanih podataka odredite snagu generatora, utrošak energije za 10 sati rada i masu nastalog aluminija.
Snaga generatora pri radu na 40 kupatila P = U • I = 40 • 7 • 5000 = 1400000 W = 1400 kW.
Električna energija potrošena za 10 sati, A = P • t = 1400 kW 10 h = 14000 kW • h.
Dobivena količina aluminija G = 14000:25 = 560 kg.
Na temelju teorijskog elektrokemijskog ekvivalenta, količina dobivenog aluminija trebala bi biti jednaka:
GT = A • I • t = 0,093 • 5000 • 40 • 10 • 3600 = 0,093 • 720 000 000 mg = 669,6 kg.
Učinkovitost elektrolitičke instalacije jednaka je: Učinkovitost = G / GT = 560 / 669,6 = 0,83 = 83%.